近日,青島科技大學生物工程學院顧玉超教授團隊與中國科學院微生物研究所王為善研究員團隊合作,在國際權威期刊《Journal of Controlled Release》(中國科學院一區,Top期刊)在線發表了一項關于癌癥免疫治療的最新研究成果。該研究題為“EngineeringEscherichia coliNissle 1917 to scavenge lactate enhances anti-tumor immunity”(工程化大腸桿菌Nissle 1917清除乳酸增強抗腫瘤免疫)。
該研究首次揭示了乳酸代謝是益生菌大腸桿菌Nissle 1917(EcN)發揮抗腫瘤活性的關鍵機制,并成功構建了一種具有超強乳酸代謝能力的工程化菌株BELAC。該菌株能高效清除腫瘤微環境中的乳酸,逆轉免疫抑制狀態,顯著激活機體抗腫瘤免疫反應,為開發新一代安全、高效的細菌免疫療法提供了全新的策略和理論依據。
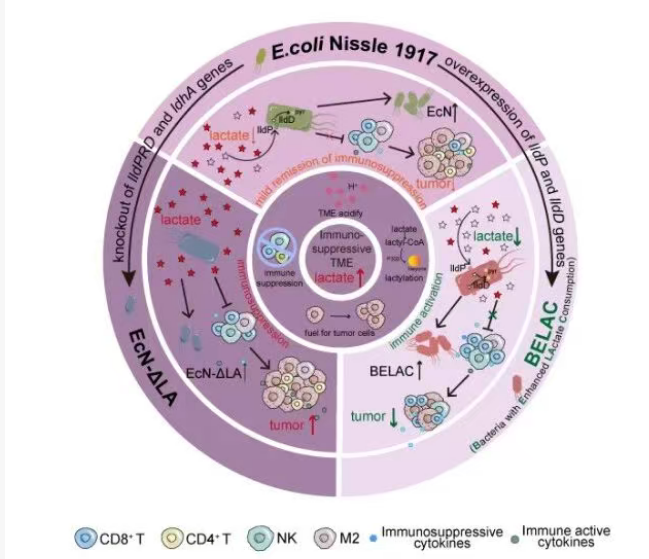
據介紹,腫瘤細胞即使在氧氣充足的情況下,也傾向于通過糖酵解進行葡萄糖代謝,同時產生大量乳酸,這一現象被稱為“瓦博格效應”。高濃度的乳酸不僅酸化腫瘤微環境,還是一種強效的免疫抑制分子,它能直接抑制殺傷性T細胞的功能,促進免疫抑制細胞的聚集,從而幫助腫瘤細胞逃避免疫系統的攻擊。
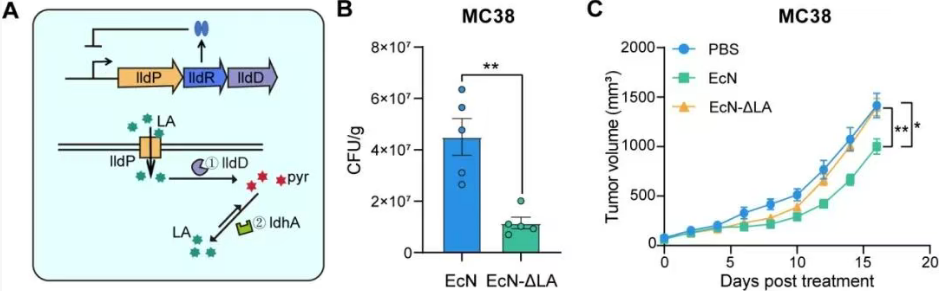
團隊采用基因組整合策略,將強化后的乳酸代謝基因盒穩定整合到EcN染色體中,成功構建了一株無質粒、基因組穩定、具有超強乳酸代謝能力的工程菌株,命名為BELAC(Bacteria with Enhanced LActate Consumption)。在B16、MC38和CT26等多種小鼠同源腫瘤模型中,BELAC展現出優異的抗腫瘤效果和安全性。值得注意的是,研究也客觀指出,在免疫原性極低的“冷”腫瘤(如4T1乳腺癌)模型中,單靠清除乳酸尚不足以完全抑制腫瘤,這提示未來可將BELAC與免疫檢查點抑制劑等療法聯用,以攻克更難治的腫瘤類型。
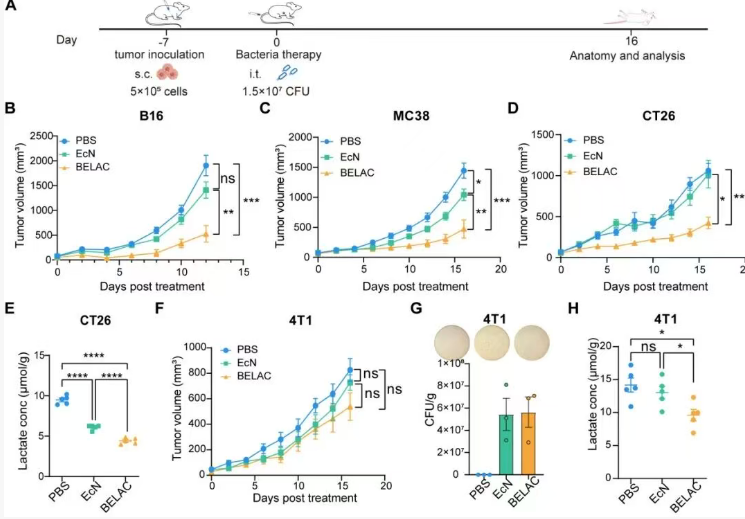
這項研究不僅闡明了EcN抗腫瘤的代謝基礎,更通過b增強細菌自身對乳酸的代謝功能實現了對腫瘤微環境的原位、持續調控,從而實現腫瘤免疫抑制微環境的重編程。更重要的是,BELAC菌株具有良好的遺傳穩定性和安全性,未來可作為“底盤”細胞,為癌癥治療提供了一種可臨床轉化的通用平臺,進一步聯合其他免疫療法,為癌癥患者帶來新的希望。
該研究得到了國家自然科學基金、國家重點研發計劃、山東省海洋科技基金及泰山學者項目等多項資助。
青島財經日報/首頁新聞記者 國瑾
責任編輯:王海山




請輸入驗證碼